产品新闻
单光子计数共聚焦显微镜系统Luminosa
日期:2023-04-10
——新型基于单分子级别荧光共振能量转移(smFRET)的动态结构生物学共聚焦显微镜系统

量化单分子和时间分辨荧光技术,为很多生命科学与材料科学领域提供了新的视野。迄今为止,因为其数据采集和分析需要具备较为专业的背景知识,使得该技术的普及非常缓慢。现在,PicoQuant可以提供一款全新的共聚焦显微系统——单光子计数共聚焦显微镜系统Luminosa,它具备先进的软硬件组合,在简化日常操作流程的前提下,能有效的为操作者呈现高质量的实验数据。其配备的软件为每种应用技术都设定了标准化的引导操作流程。
本文将为您介绍单光子计数共聚焦显微镜Luminosa系统如何简化单分子荧光共振能量转移(smFRET)的实验过程。
单光子计数和计时应用开启了一个全新的实验维度
共聚焦荧光显微镜在过去四十年中越来越受欢迎,因为其可视化动态过程和细胞结构,使其成为一种用于分子、细胞和发育生物学的常规主力仪器。除了成像之外,点测量相关的实验方法,例如荧光相关光谱(FCS)和单分子荧光共振能量转移(smFRET)也在生物物理学领域日渐普及。最近发展起来引入时间分辨的实验方法更是颇为引人注目。对荧光基团荧光寿命的测量,揭示了新的信息维度,可以和光谱信息相互补充。每个荧光基团的荧光寿命信息是独特的,因此可以作为多重检测的识别特征。它同时也可以被单分子间的荧光共振能量转移所影响,例如,由于受体的存在导致供体寿命下降而反应出的荧光共振能量转移效率。
迄今为止,使用时间分辨荧光技术的门槛相对较高,需要专业的背景知识。而全新的单光子计数共聚焦显微镜系统Luminosa大大降低了使用门槛,并且将多种时间分辨工具集成统一。并为以下研究领域提供新的视野:
▪单分子级别的动态结构生物学
▪相位分离引起的细胞机制
▪环境监测
▪细胞膜的动态和结构成像
▪功能性的纳米囊泡特性检测
▪研究单分子级别下的化学反应
▪先进材料的特性表征
▪质量和稳定性检测
在这些研究领域中,实验复现是一个难题。可能的原因之一在于所使用的显微方法的细节描述不充分。为了提升准确性,可重复性以及实验质量,通过显微系统的自动化来减少人为误差是一个潜在的可行方案,例如,硬件部件的自动化,以及将传感单元集成到智能软件中。这也增加了成像系统的易用性,总而言之,为研究人员节省了宝贵的时间和材料。此外,自动化提高了通量,甚至开辟了新的实验可能性,如延时成像、多位置成像或多点时间轨迹。
直观的工作流程,易于使用
单光子计数共聚焦显微镜系统Luminosa在寿命测量领域有着最佳的性能表现。该显微系统同样对于单分子灵敏度进行了优化,可以进行单分子级别的各种实验。我们通过MicroTime200系统的实验经验设计了这个全新的显微镜系统,并为它挑选了一批最佳硬件组合。通过精简和优选后的光学元件使得该系统达到了极高的灵敏度水平。用户既可以选择使用高速的振镜系统进行扫描成像,也可以一键切换为压电平移台的物镜扫描模式。这种切换功能目前在其他显微系统中是没有的。压电扫描成像避免了振镜扫描模式下的信号损失,根据波长的不同,大约可以提升20-30%左右的光子信号。用户同时也可以选择时间响应更优秀的混合式光电倍增管探测器,或者高探测灵敏度的单光子雪崩二极管作为定制配置。
超简单的界面操作流程
单光子计数共聚焦显微镜系统Luminosa软件是从头开始创建的。它的设计使其工作流程简单快捷,使用户能够更加专注于样品特性本身。良好的交互界面布局,清晰排列的界面仅显示与每个应用相关的参数,保证了测量数据的重复精度。单光子计数共聚焦显微镜系统Luminosa软件包括smFRET功能,FCS荧光相关光谱,以及时间分辨成像功能,同时也具备有自定义测量和分析模式。系统只需单击一个按钮,在不到一分钟的时间内,便可完成无样品自动对准。对准非常准确,无需进一步优化即可直接进行FCS荧光相关光谱测量,所以通过简单的操作就可以确保系统始终处于相同的最佳状态。
开始操作时,用户选择在下一个实验中使用哪种测量技术方法。软件中清晰排列的软件界面仅显示该类型测量所需的参数,从而将意外错误的风险降至最低。根据选择样品中存在的荧光团,硬件会自动正确配置。然后根据实验环境分配分析通道。大多数商用LSM共聚焦显微系统中已经提供了类似的功能,但是现在还设置了对时间分辨测量很重要的其他参数(例如激光的重复频率),从而减少对用户所需专业知识的要求。设置的保存和加载,保证了测量的可重复性。此外,适当的原始数据与实际数据一起保存,方便以后查询使用。
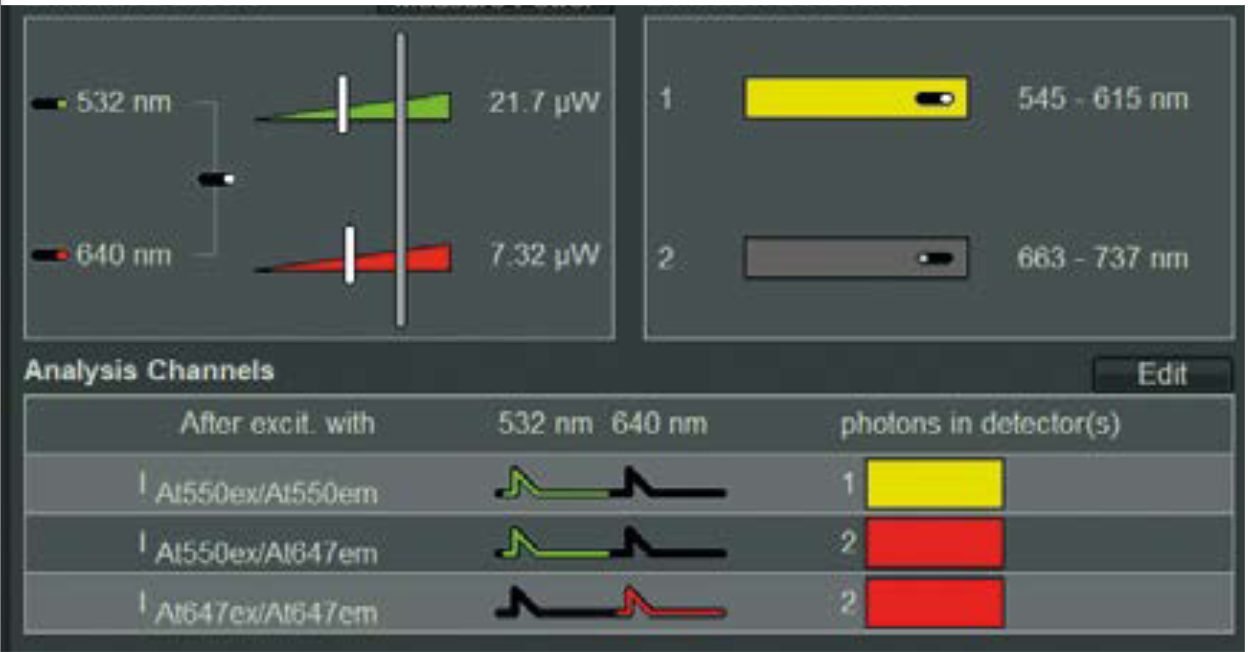
图2. 使用532nm和640 nm脉冲交错激发和双通道检测的smFRET实验的硬件和分析设置屏幕截图,产生三个逻辑分析通道。
激发光的功率校准模块同时可以提供设置和显示激发功率(单位μw,如图2)的功能,并且不需要额外的功率测量设备。自动调节耗时不到十秒,而且可以在不移动样品的情况下连续进行。参考文献[2]表明了激发光强的精确控制在可重复精度中的重要性,例如它会影响到光漂白,光毒性等等,从而在结果中引入不确定性。 这个问题对实验的影响非常大, QUAREP - LiMi (光显微镜质量和重复精度评估组织)也将激发光功率的控制放在工作的首位。
在实验进行测量时,会实时显示多个在线预览。这样用户就可以把控样品的情况,从而进一步进行正确的采集参数设定。在线实时分析实际上是一种动态帮助信息,旨在提高采集到的数据质量。
新软件结合了用于荧光寿命成像(FLIM),荧光相关光谱(FCS)和单分子检测的GPU加速算法。 强大的算力使得其可以实现自动分析程序,并将有关实验类型、硬件配置、荧光团和数据维度的信息考虑在内,因此无需用户交互即可获得初始结果。尽管如此,原始数据保持不变,以便于以后可以使用不同的参数设置重新分析。
基于动态结构生物学的单分子荧光共振能量转移(smFRET)
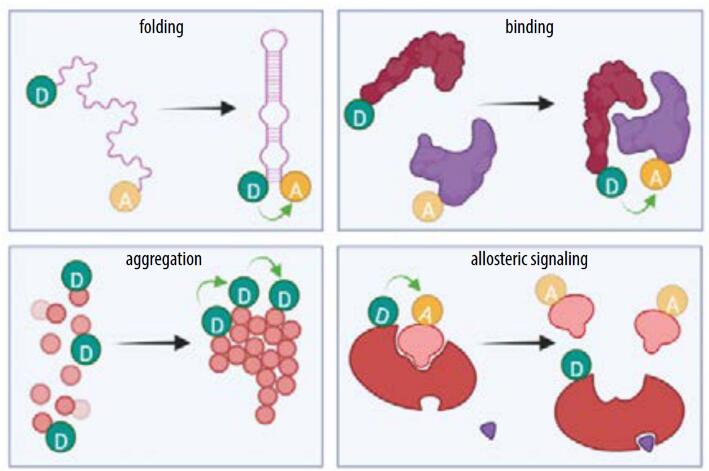
图3. 典型的smFRET应用 - 研究蛋白和DNA的作用(图片来自biorender.com)
单分子研究,以及更具体的smFRET方法学,已成为研究蛋白质和核酸动态结构变化的标准工具。这些实验方法可以揭示在纳秒到秒级别的时间维度上的动态活动过程。例如成链动力学,蛋白的结合,折叠,探测变构信号,寡聚化以及聚集现象,如图3所示。实验结果对其他实验方法,例如电镜,核磁共振等,进行了有效的补充。这样完整的数据就可以被归档到到综合结构模型的存档系统PDB-Dev [3]。近年来,内在无序蛋白质的生物学相关性研究越来越多,突出了这些方法的力量。
smFRET测试既可以在分子自由移动的溶液中进行,也可以对分子固定在盖玻片表面上的样品实施探测。单光子计数共聚焦显微镜系统Luminosa为两种样品分别提供了专门的工作流程。
选择正确的FRET对信息后,硬件会自动切换到对应的配置,即设置激发波长和功率,启用供体和受体的脉冲交错激发,并选择正确的检测器和发射滤光片,如图2所示。此外,系统会根据实验条件选择分析通道:供体激发后的供体发射,供体激发后的敏化受体发射和直接受体激发后的受体发射作为对照。可以选择不同的停止条件进行采集。例如,在分子溶液样品测试时,停止条件可以是爆发发射数量、总时间、爆发频率的减少量等等。这有助于收集具有充分统计数据的一致数据集。
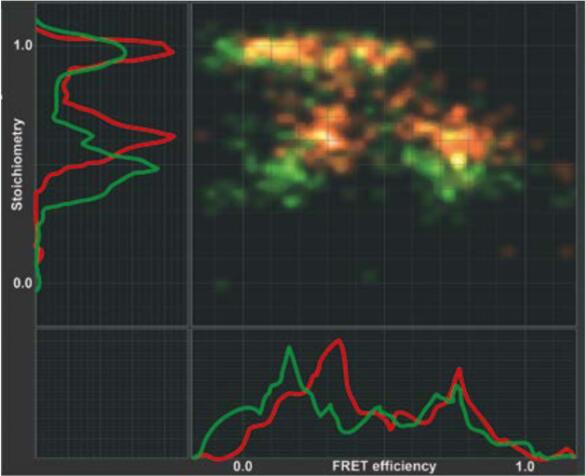
采集数据时会显示四种在线数据预览: FRET效率(E)与化学计量(S)的直方图、爆发直方图、强度时间轨迹和TCSPC直方图,以及用于供体和受体寿命衰减的在线拟合。E和S在线计算并显示在E/S直方图中。根据[4]中的数据处理标准步骤,这些在线数据通过四种因子进行校正。这些校正因子分别是:光谱串扰因子α,激发波动因子β,探测效率因子γ以及直接激发因子δ。校正后以及未校正数据都在图4中有所显示,这样就可以评估校正步骤带来的影响,这些因子在随后都可以手动进行修改。
分子穿过固定的激光聚焦光斑时,所发出的荧光信号被采集。这些信号可以连同共聚焦针孔大小来确定聚焦光斑的体积。观察时间窗口,例如,爆发持续时间是由聚焦体积来决定的。在衍射极限级别的聚焦体积下,极短时间内就有高量级的光子产出,可以被用于监控快速的分子动态过程。增大聚焦体积的同时会延长爆发持续时间,如图5所示。这样就可以观察慢速分子的动态过程和测量大分子较缓慢的扩散特性。总体上说,如[5]中表述的,“更大的聚焦体积,结合高功率的激发,每个爆发持续时间能产出最高的光子量级”。单光子计数共聚焦显微镜系统Luminosa能够根据激发波长的不同,将观察体积从衍射极限的3倍增加到6倍。在软件中点击一个按钮,可以减小激发光束直径,对物镜进行下充,相应调整光路和共焦探测针孔的大小,从而增加有效观测体积。
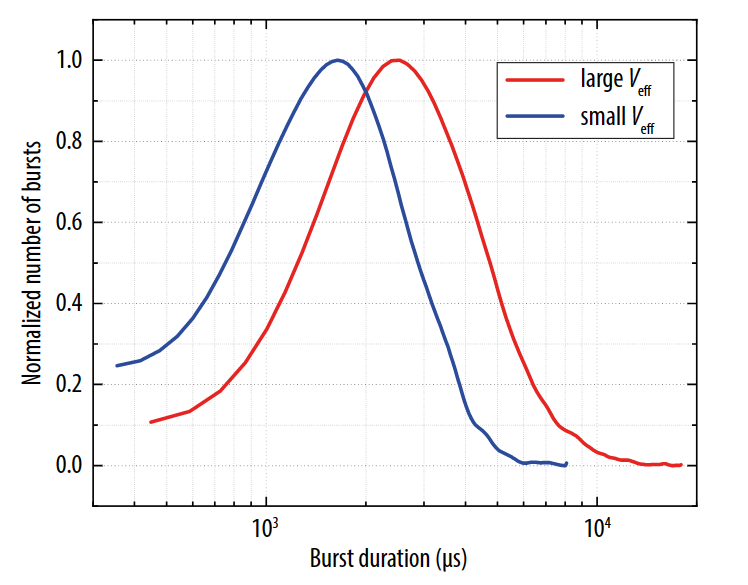
图5. 爆发持续时间对比图,红色为较大聚焦体积下,蓝色为较小聚焦体积下。
在研究分子固定在表面的样品时,用户既可以选择压电扫描台来获得更多的光信号,也可以选择振镜扫描方式来快速成像。样品自动保持对焦,而平铺和拼接可实现大面积成像,如图6所示。
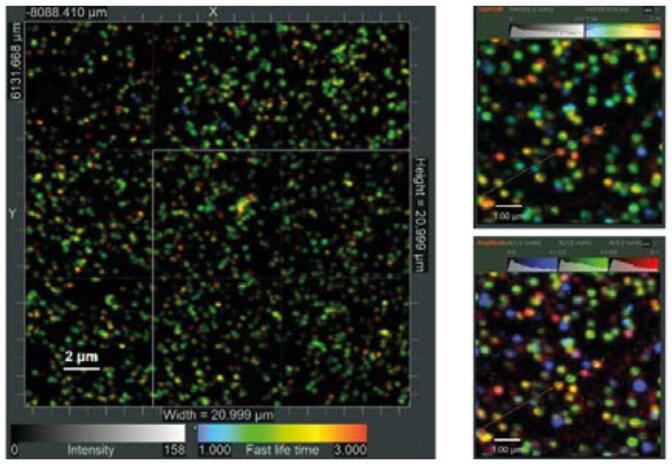
图6. 用Cy3B和Atto647N标记的单DNA折纸固定在表面上。九张成像图片拼接成了一张21x21µm的图像。右图:单张小图的FLIM分析结果。上图:平均寿命图。下图:多指数寿命拟合结果叠加图。样品数据由弗里堡大学,物理学院提供。
采集到一个成像图块后,通过自动算法在特定标准下,测算出单分子的位置。随后对这些单分子进行逐个探测,并在停止条件达到之前记录其光强随时间变化的数据。然后,下一个图块区域将被扫描和成像,以此类推。通过这种方式,可以轻松获得具有足够统计数据的数据集。
讨论和展望
单光子计数共聚焦显微镜系统Luminosa的自动化工作流程提高了系统的易用性并减少了人为错误,从而节省了研究人员的宝贵时间和样品材料。重要的是,自动设置的参数值可以保存为元数据,而在手动系统中,必须手动记录这些值。综上所述,与手动操作的系统相比,该系统提高了实验的精确度、可重复性和实验质量。但是,审查配置和设置(例如染料数据库条目或丢弃事件的阈值)以确保它们适合新实验仍然是很重要的。许多专业的知识应用于制定系统的工作流程和参数设定中,所以实际使用人员并不需要具备相关专业知识。即便如此,在样品制备和数据阐释方面,用户仍然需要一定的知识储备。
PicoQuant持续研发新的荧光显微镜科研工具,例如光谱分辨FLIM系统,结合了寿命和光谱信息,可同时并行多目标成像,详情参阅文章[6]和[7]。PicoQuant同时活跃于各种与学术界合作的研究项目中,来拓展新型显微系统的概念和实验方法。例如,NG-FLIM计划,旨在实现一种高空间分辨率和高时间分辨率的显微系统,这样可以更加简便和精确的在活体细胞和组织中快速观察膜受体的情况。不同的光学方法再结合起来以提高成像的对比度,基于深度学习的数据处理方式用于自动化的数据评估。这项计划的参与者包括PicoQuant、Nanotag Biotechnologies、Arivis、哥廷根大学以及哥廷根中心医药大学。该计划由德国联邦教育和研究部的”Photonics Research in Germany”项目(项目编号 13N15324)拨款。另一个例子就是纠缠态的双光子吸收,可以被应用于化学选择性荧光显微镜。PicoQuant正与弗劳恩霍夫应用光学和精密工程研究所、M Squared Lasers以及耶拿大学一起合作研究此主题。该方向同样由德国联邦教育和研究部支持,隶属于LIVE2QMIC(13N15953)研究项目。
结论
PicoQuant的新型单光子计数共聚焦显微镜系统Luminosa可以帮助研究者轻松的将单分子时间分辨荧光显微实验方法广泛应用于生命和材料科学研究领域,而不需要操作者本身具备丰富的经验。得益于新的软件功能与最先进的硬件相结合,并且更好地集成了硬件和软件,该系统以可重复的方式快速提供高质量的数据。这使研究人员能够自信地采用smFRET等新方法,从新的角度观察样品。[1] M.Baker: 1,500 scientists lift the lid on re-producibility,Nature 533 (2016) 452–454。
[2] P.Montero Llopis et al.: Best practices and tools for reporting reproducible fluores-cence microscopy methods,Nat Methods 18 (2021)1463–1476。
[3] E.Lerner,A. Barth,J.Hendrix et al.: FRET-based dynamic structural biology: Challenges, perspectives and an appeal for open-science practices.Ashok.(2021) eLife 10:e60416。
[4] B.Hellenkamp,S.Schmid,O.Doros-henko et al.: Precision and accuracy of single-molecule FRET measurements – a multi-laboratory benchmark study,Nat Methods 15 (2018) 669–676。
[5] G.Agam,C.Gebhardt,M.Popara et al.: Re-liability and accuracy of single-molecule FRET studies for characterization of struc-tural dynamics and distances in proteins.(2022)bioRxiv 2022.08.03.502619。
[6] T.Niehörster et al.: Multi-target spectrally resolved fluorescence lifetime imaging mi-croscopy,Nat Methods 13 (2016) 257–262。
[7] S.Rohilla et al.: Multi-target immuno-fluorescence by separation of antibody cross-labelling via spectral-FLIM-FRET,Sci Rep 10 (2020) 3820。